衝撃波の科学寄稿 高山 和喜 氏
第4回:衝撃波の医療応用
2006/08
32. レーザーアブレージョンドラッグデリベリー
固体の微粒薬剤を患部あるいは生体に注入する技術はドラッグデリベリー(drug delivery system, DDS)と総称され、最近の医工学の熱い話題の一部である。好ましい特性を持つ遺伝子を細胞内に導入して既存の遺伝子と組み替える技術が開発されている。導入法として組み替え遺伝子をヴィールスあるいは、リポゾーム、二重膜を持つ脂肪酸、に取り込ませて標的細胞中に導入するなど、種々の技術が提唱されているが、導入率は高くない。
一方、物理的に遺伝子を細胞中に打ち込む技術が提唱され、生物学的な手法に比べて導入率が高い。1978年クラインは火薬銃で前面に組み替え遺伝子を貼り付けた飛行体を加速し、銃口で飛行体を急停止させたとき、微粒子のみが慣性で自由飛行して標的細胞に貫入する方式を提出した。植物細胞の遺伝子組み換えを目指して、デュポン社は、高圧ヘリウムの解放で発生する衝撃波とその背後の高速流れを用いて遺伝子を塗布した金属粒子を加速し、直接標的細胞に打ち込む技術を開発した。この装置は実用化され商品名バイオリスティック(Biolistic)で市販されている。北アメリカの組み替え遺伝子作物は、殆どこの装置で処理された成果とも言われている。
 日本の農林省がこの技術の重要さに気付いたときは、この装置に変わる発明は日本になく、バイオリスティックの成果を傍観した。その後、物理的に微粒子を加速して細胞に打ち込む方法は種々提案されているが、実用技術に結びつくものは少なく、医療への展開は無かった。1997年、オックスフォード大学のベルハウスはカプセルに封じ込めた高圧ヘリウムを駆動源に固体微粒子を加速して皮膚に打ち込む装置を開発し、非接触的な注射器、商品名パウダージェクト(Powder Ject)を実用化した。
日本の農林省がこの技術の重要さに気付いたときは、この装置に変わる発明は日本になく、バイオリスティックの成果を傍観した。その後、物理的に微粒子を加速して細胞に打ち込む方法は種々提案されているが、実用技術に結びつくものは少なく、医療への展開は無かった。1997年、オックスフォード大学のベルハウスはカプセルに封じ込めた高圧ヘリウムを駆動源に固体微粒子を加速して皮膚に打ち込む装置を開発し、非接触的な注射器、商品名パウダージェクト(Powder Ject)を実用化した。
2000年、金属膜にQ-スイッチレーザー光を照射すると、高エネルギー蓄積で金属表面は瞬間的に超高温に曝され、レーザー光照射と逆方向に金属プラズマジェットを噴出し、その反作用として金属中には衝撃波が伝播する。プラズマジェット発生は融除、アブレージョン(ablation)と呼ばれ、航空宇宙工学では宇宙船の大気圏再突入で宇宙船の先端が強い衝撃波に曝されて融ける現象なので、衝撃波研究者には馴染みの物理だった。
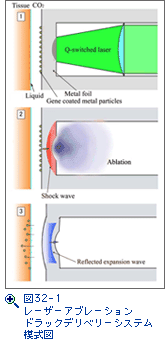
金属膜中を伝播する衝撃波は裏面の空気界面で膨張波となって反射し、金属膜は瞬間的に変形することに注目して、我々はレーザーアブレージョンをドラッグデリベリーに結びつける研究を開始した。金属膜変形速度はレーザー光のエネルギー密度と膜厚さにもよるが、容易に1~3km/sに達するので、金属膜の裏面に直径1μm程度の微粒子を貼り付けると、金属膜変形はカタパルトのように微粒子を1km/s程度の速度で吹き飛ばされて、容易に標的の生体に突入する(図32-1)。
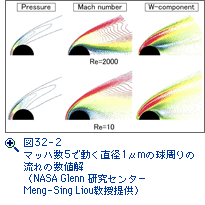 直径1μmの微粒子が1~2km/sで自由飛行する現象のレイノルズ数は10以下、マッハ数は5程度であり、今までの高速力学が取り扱う研究範囲から大きく逸脱している。低レイノルズ数流れはストークス流れと呼ばれ、流体力学者は、微粒子は常に微速で動くと思いこんでいたから、極超音速のストークス流れは既成概念にない領域に属する異常な流れになる。微粒子直径1μmは大気圧下の空気構成分子の平均自由行程10nmの100倍程度の大きさで、微粒子周りの流れは中間領域の希薄気体効果を示し、多少不正確になるが連続流の取り扱いを許す。図32-2は極超音速飛行する微粒子周りの流れをナヴィエ-ストークス式の数値解で模擬した結果である。このような微粒子周りの衝撃波の構造は、大きな物体周りのそれとは異なり、また、マッハ数5の極超音速流れの淀み点温度よりも低い。また、固形薬剤ないし遺伝子の飛行距離は高々数mmで、高温に曝される時間は1μs程度なので、物体表面温度が目立って上昇する前に、微粒子は標的に突入する。
直径1μmの微粒子が1~2km/sで自由飛行する現象のレイノルズ数は10以下、マッハ数は5程度であり、今までの高速力学が取り扱う研究範囲から大きく逸脱している。低レイノルズ数流れはストークス流れと呼ばれ、流体力学者は、微粒子は常に微速で動くと思いこんでいたから、極超音速のストークス流れは既成概念にない領域に属する異常な流れになる。微粒子直径1μmは大気圧下の空気構成分子の平均自由行程10nmの100倍程度の大きさで、微粒子周りの流れは中間領域の希薄気体効果を示し、多少不正確になるが連続流の取り扱いを許す。図32-2は極超音速飛行する微粒子周りの流れをナヴィエ-ストークス式の数値解で模擬した結果である。このような微粒子周りの衝撃波の構造は、大きな物体周りのそれとは異なり、また、マッハ数5の極超音速流れの淀み点温度よりも低い。また、固形薬剤ないし遺伝子の飛行距離は高々数mmで、高温に曝される時間は1μs程度なので、物体表面温度が目立って上昇する前に、微粒子は標的に突入する。
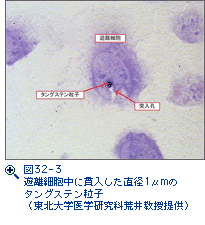 実験は裏面に直径1mmのタングステン球を貼り付けた厚さ100mmのアルミ箔にQ-スイッチNd:YAGレーザー光、パルス幅5.5ns、エネルギー1.1~1.4J、波長1.06nmを照射した。図32-3は遊離細胞に突入したタングステン粒子を示す。現在は実験系を小型で簡単な光学系に改良して内視鏡と組み合わせて人体の到達可能な部位に導入して、低侵襲的に薬剤あるいは遺伝子を打ち込む装置の実用設計が進行中である。
実験は裏面に直径1mmのタングステン球を貼り付けた厚さ100mmのアルミ箔にQ-スイッチNd:YAGレーザー光、パルス幅5.5ns、エネルギー1.1~1.4J、波長1.06nmを照射した。図32-3は遊離細胞に突入したタングステン粒子を示す。現在は実験系を小型で簡単な光学系に改良して内視鏡と組み合わせて人体の到達可能な部位に導入して、低侵襲的に薬剤あるいは遺伝子を打ち込む装置の実用設計が進行中である。
 最近、東北大学生命科学研究科菅野明助教授は共同研究の一環として、この方法を用いて、遺伝子を塗布した金微粒子を玉葱の表皮に打ち込んで、遺伝子組換えで遺伝子発現を確認した。図32-4はその結果で、青色の部分が遺伝子発現を示している。
最近、東北大学生命科学研究科菅野明助教授は共同研究の一環として、この方法を用いて、遺伝子を塗布した金微粒子を玉葱の表皮に打ち込んで、遺伝子組換えで遺伝子発現を確認した。図32-4はその結果で、青色の部分が遺伝子発現を示している。
|



